第十期:脑血管病的外科与介入治疗
Archive Date: 2026-04-04 Series: 脑血管讲义系列 Total Lectures: 10期
一、解剖与生理基础(B)
1. 颈动脉粥样硬化斑块的解剖定位
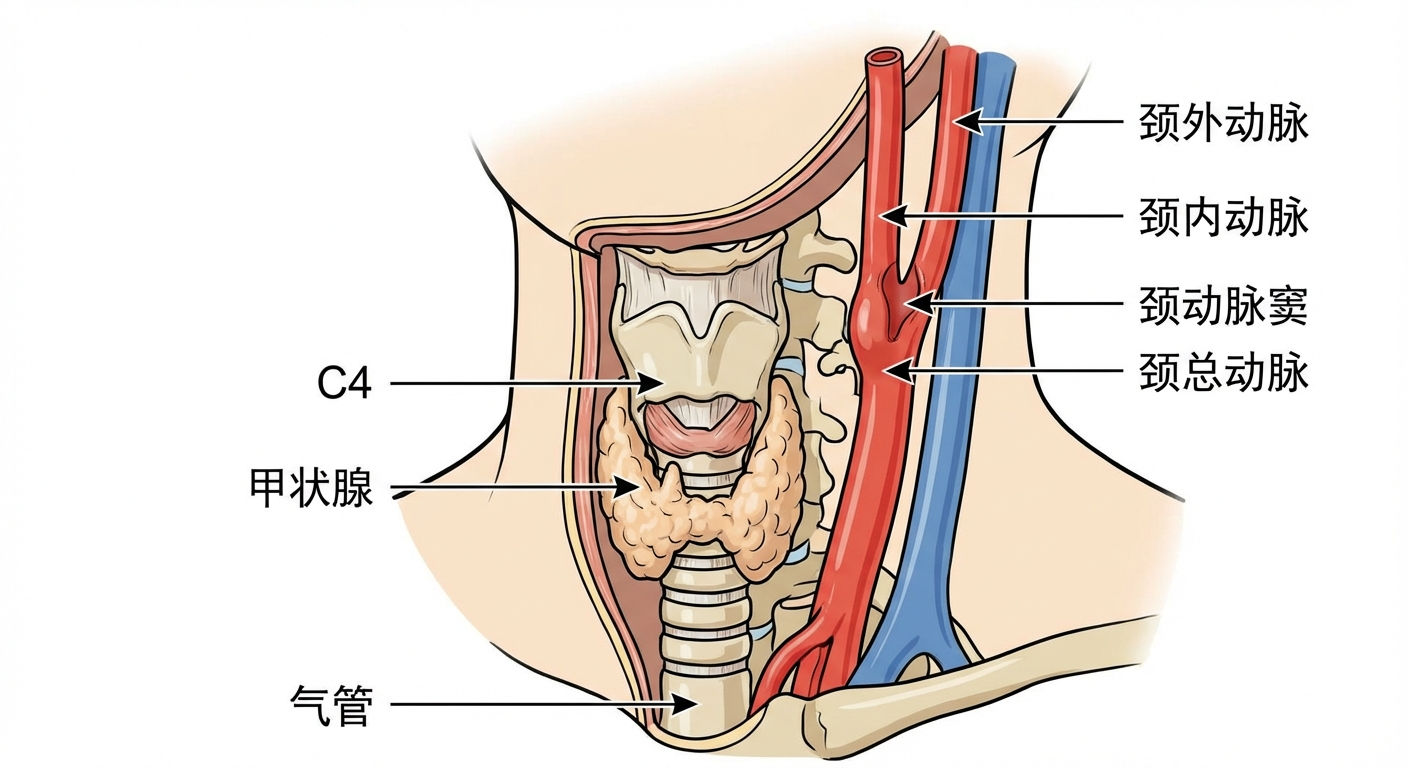
颈动脉狭窄的手术与介入治疗均基于对颈动脉分叉解剖的精确理解:
| 部位 | 供血区域 | 临床意义 |
|---|---|---|
| 颈总动脉(CCA) | — | 阻断部位:胸锁乳突肌内侧缘 |
| 颈内动脉(ICA) | 大脑中/前动脉流域 | 眼动脉以上为"安全阻断区" |
| 颈外动脉(ECA) | 面部/头皮侧支 | 术中可作为临时分流通道 |
| 颈动脉球部(Bulb) | 湍流高发区 | 粥样硬化最常见部位 |
| ICA远端(岩骨段/床突段) | Willis环前向供血 | CAS释放支架的关键区域 |
侧支循环评估:术前需通过CTA/MRA评估Willis环完整性。若前交通动脉缺失,CEA术中需考虑是否需要转流:
颈动脉阻断试验:
阻断ICA → 测量远端反流压力(Stump Pressure)
└─ >50mmHg → 可安全阻断(无需转流)
└─ <50mmHg → 建议转流管置入
2. 颅内动脉瘤的解剖学基础
颅内动脉瘤的发生与血流动力学密切相关,好发部位遵循特定解剖规律:
| 部位 | 占比(约) | 备注 |
|---|---|---|
| 前交通动脉(Acom) | 30% | 最常见破裂部位 |
| 后交通动脉(Pcom) | 25% | 胚胎型后交通相关 |
| 大脑中动脉分叉(MCA Bif) | 20% | 巨大动脉瘤好发 |
| 基底动脉尖 | 5% | 高流量,介入困难 |
| 其他 | 20% | 多发/串联动脉瘤 |
动脉瘤壁结构:颅内动脉瘤壁缺乏外弹力层,仅由内皮+平滑肌+纤维膜构成,是介入治疗的解剖学基础。
3. 机械取栓的解剖路径
机械取栓的入路解剖是介入治疗的核心:
股动脉入路 → 主动脉弓 → 颈总动脉 → 颈内动脉 → 颅内动脉
┌─ 大脑中动脉( M1/M2段)
颈内动脉 → 眼动脉开口上方
└─ 大脑前动脉( A1段)
关键弯曲:
Ⅰ型主动脉弓 → 操作简单
Ⅱ型(牛型弓) → 导管到位困难
Ⅲ型 → 需要长鞘/中间导管
二、病理机制(P)
1. 颈动脉狭窄的病理进展
颈动脉粥样硬化是外科与介入治疗的主要适应证,其病理进展决定治疗时机:
| 病理阶段 | 狭窄程度 | 斑块性质 | 治疗策略 |
|---|---|---|---|
| 轻度狭窄 | <50% | 稳定斑块 | 药物治疗(最新研究对重度狭窄也趋向积极) |
| 中度狭窄 | 50-69% | 混合斑块 | 药物治疗为主,症状性可考虑CEA |
| 重度狭窄 | ≥70% | 不稳定斑块、溃疡 | CEA或CAS首选 |
| 近乎闭塞 | 99% | 线样征 | 介入治疗难度高,需评估 |
易损斑块(Vulnerable Plaque)特征:
- 薄纤维帽(<65μm)
- 大脂质核心(>40%斑块体积)
- 活跃炎症(巨噬细胞浸润)
- 斑块内出血(IPH)
- 新生血管形成
⚠️ ACST-3/CREST-2研究新进展:无症状性重度狭窄(≥70%)在围术期并发症<3%的前提下,CEA优于单纯药物治疗。
2. 脑出血的病理分型与手术指征
脑出血手术治疗的选择基于血肿扩大风险与病理分型:
| 出血类型 | 病因 | 血肿特点 | 手术指征 |
|---|---|---|---|
| 高血压性脑出血(HICH) | 豆纹动脉/穿支 | 基地节/丘脑/桥脑 | 幕上>30ml伴神经功能恶化 |
| 淀粉样血管病(CAA) | 皮层/软脑膜动脉 | 脑叶,多发微出血 | 手术需慎重,倾向保守 |
| 血管畸形 | AVM/海绵状血管瘤/DAVF | 部位不定 | 反复出血史者考虑 |
| 肿瘤卒中 | 转移瘤/胶质母细胞瘤 | 环形强化 | 活检+肿瘤治疗 |
血肿扩大的时间窗:75%血肿扩大发生于发病3小时内,6小时内是外科干预的黄金窗口。
3. 动脉瘤破裂出血的病理
颅内动脉瘤破裂引起蛛网膜下腔出血(SAH),其病理过程决定治疗紧迫性:
动脉瘤破裂 → SAH → 脑血管痉挛 → 迟发性脑缺血(DCI)
↓ ↓
早期再出血(24h内 3-4%) 3-14天高峰期
Hunt-Hess分级与手术耐受性:
| 分级 | 意识状态 | 症状 | 手术时机建议 |
|---|---|---|---|
| Ⅰ | 无症状/轻微头痛 | 轻度颈强 | 早期(0-3天) |
| Ⅱ | 中度头痛 | 颈强,无神经缺损 | 早期(0-3天) |
| Ⅲ | 昏睡 | 轻度局灶体征 | 早期,但需ICU稳定 |
| Ⅳ | 昏迷 | 中-重度偏瘫 | 延迟至稳定 |
| Ⅴ | 深昏迷 | 去脑强直 | 保守或紧急减压 |
三、分子与影像(M)
1. 颈动脉影像评估
精准影像评估是外科/介入治疗决策的前提:
| 影像方法 | 评估内容 | 优势 | 局限 |
|---|---|---|---|
| CTA | 狭窄率、斑块形态、溃疡 | 快速、广泛可用 | 碘对比剂、辐射 |
| MRA(TOF/CE) | 狭窄率、斑块成分 | 无创、无辐射 | 假阳性偏高 |
| DSA(金标准) | 狭窄率、侧支、斑块形态 | 最高分辨率 | 有创、辐射 |
| 颈动脉超声 | IMT、斑块回声、流速 | 床旁、无创 | 操作者依赖 |
| 高分辨MRI(HR-MRI) | 斑块成分(纤维帽/IPH) | 软组织分辨率最高 | 耗时、不可用急诊 |
狭窄率测量方法(NASCET标准):
狭窄率 = (1 - 狭窄处残腔内径 / 正常远端ICA内径) × 100%
正常ICA(远离斑块处)→ D
狭窄最重处 → d
狭窄率 = (1 - d/D) × 100%
├─ <50% → 轻度(药物治疗)
├─ 50-69% → 中度(症状性考虑CEA)
└─ ≥70% → 重度(CEA/CAS指征强烈)
2. 机械取栓的影像评估
急性缺血性卒中机械取栓前需通过影像筛选患者:
| 检查 | 目的 | 时间要求 | 关键指标 |
|---|---|---|---|
| NCCT | 排除出血、评估ASPECTS | <10分钟 | ASPECTS≥6 |
| CTA | 判断大血管闭塞(LVO) | 与NCCT同步 | M1/M2/ICA-T/BA闭塞 |
| CTP | 评估核心梗死/不匹配 | 可选 | 核心<70ml,不匹配>1.8 |
| MRI-DWI | 精准核心梗死 | 时间允许时 | 梗死核心体积 |
| DSA | 确认+治疗 | 直接至导管室 | 侧支评分(ACS) |
ASPECTS评分:
评分区域(10分):
M1-M6各1分 + Cingu + Insula + Lentiform + ICA分布
≥6分 → 溶栓+取栓获益明确
0-5分 → 取栓需个体化评估(梗死太大)
3. 颅内动脉瘤的影像评估
| 影像方法 | 评估内容 | 优先级 |
|---|---|---|
| CTA | 动脉瘤大小/位置/瘤颈 | 急诊首选 |
| MRA(3D-TOF) | 无创筛查/随访 | 随访首选 |
| DSA(3D-DSA) | 精确测量/分型/血管痉挛 | 金标准+治疗 |
| 高分辨MRI | 动脉瘤壁强化/夹层 | 研究/分型困难时 |
动脉瘤测量参数:
- 瘤体直径(Fundus)
- 瘤颈宽度(Neck)
- 宽/窄颈分界:瘤颈≥4mm 或 瘤颈/瘤体比>1/2 → 宽颈
- 体颈比(S/N Ratio)→ <1.5 为宽颈,介入难度高
四、临床表现与治疗指征(R)
1. 颈动脉血运重建的指征
CEA(颈动脉内膜切除术)指征:
| 类别 | 狭窄程度 | 其他条件 |
|---|---|---|
| 有症状性 | ≥70% NASCET | 6个月内TIA/卒中 |
| 有症状性 | 50-69% NASCET | 亚组患者可获益 |
| 无症状性 | ≥70% NASCET | 围术期并发症<3%,预期寿命>5年 |
CAS(颈动脉支架)适应证:
| 情况 | 推荐级别 |
|---|---|
| 高外科风险CEA | 颈动脉蹼/纤维肌性发育不良 |
| 放疗后狭窄 | 手术粘连解剖困难 |
| 对侧喉返神经麻痹 | CEA风险高 |
| 串联病变(需同期处理) | 颅内/椎动脉同期治疗 |
| 解剖变异 | 颈动脉高位分叉/颈椎活动受限 |
CEA vs CAS 比较:
| 指标 | CEA | CAS |
|---|---|---|
| 围术期卒中 | 更低(症状性) | 稍高 |
| 心肌梗死风险 | 稍高 | 更低 |
| 颅神经损伤 | 3-5% | 无 |
| 血肿/穿刺并发症 | 局部血肿 | 穿刺血肿/夹层 |
| 再狭窄率 | 更低 | 稍高 |
| CAS适合患者 | 高手术风险解剖变异 | 老年(>75岁)相对倾向CAS |
2. 机械取栓的指征
符合EXTEND/DAWN标准的患者(发病6-24小时):
| 标准 | 条件 |
|---|---|
| 年龄 | ≥18岁 |
| 基线NIHSS | ≥10 |
| 核心梗死 | ASPECTS≥6 或 CT/CTA显示<50%MCA区域 |
| LVO部位 | ICA-T/ MCA-M1/BA |
| 侧支 | ACS≥2 或临床-影像不匹配 |
机械取栓主要技术:
| 技术 | 原理 | 适应 |
|---|---|---|
| ADAPT(直接吸引) | 导管抽吸 | 首选技术,首过再通率高 |
| SR(支架取栓) | Solitaire/ Trevo支架 | 首选或补救 |
| SWIM(Solumbra) | 支架+抽吸结合 | 复杂病变 |
| BADDASS | 全程球囊导引导管+双吸+支架 | 高负荷血栓 |
首过效应(FPE):首次取栓即实现mTICI 2b-3,与良好预后强相关。
3. 脑出血的手术指征
| 出血部位 | 手术指征 | 推荐术式 |
|---|---|---|
| 基底节/壳核 | 血肿>30ml,GCS≤12 | 显微镜下血肿清除+去骨瓣减压 |
| 丘脑 | 血肿>15ml伴脑积水/神经恶化 | 脑室引流→内镜血肿清除 |
| 小脑 | 血肿>15ml或>3cm,脑干受压 | 枕下开颅+血肿清除 |
| 脑叶 | 血肿>30ml,距皮层<1cm | 锁孔开颅/内镜 |
| 脑室出血 | 铸型性脑室出血 | EVD+脑室内溶栓(rtPA/q12h×3) |
⚠️ STICH系列研究结论:开颅手术在总体人群中未显示获益,但亚组分析(表浅血肿、脑疝前期)可受益。
4. 颅内动脉瘤的治疗指征
| 情况 | 处理策略 |
|---|---|
| 破裂动脉瘤(aSAH) | 早期处理(24-72h内)→ 介入首选(根据解剖) |
| 未破裂动脉瘤(UIA) | PHASES评分≥5 → 积极处理 |
| 巨大动脉瘤(>25mm) | 血流导向装置(FD)或复合手术 |
| 血泡样动脉瘤 | 血管内治疗优先(支架辅助/FD) |
介入技术选择:
| 技术 | 原理 | 适应 |
|---|---|---|
| 弹簧圈栓塞(Coiling) | 铂金弹簧圈填塞瘤腔 | 窄颈动脉瘤首选 |
| 球囊辅助栓塞(BAC) | 球囊暂时封堵瘤颈 | 宽颈/破裂急性期 |
| 支架辅助栓塞(SAC) | 支架保护瘤颈 | 宽颈、梭形 |
| 血流导向装置(FD) | 血流重构,促进瘤内血栓 | 巨大/复杂动脉瘤 |
| Web(扰瘤装置) | 瘤内扰流 | 分叉部宽颈动脉瘤 |
五、治疗原则与关键技术(C)
1. CEA 手术原则
标准CEA步骤:
① 体位:仰卧,肩垫,颈部轻度过伸对侧偏
② 切口:胸锁乳突肌前缘纵向切口
③ 暴露:依次显露CCA→ECA→ICA→舌下神经(保护)
④ 阻断:阻断顺序:ECA→CCA→ICA(反来之!)
⑤ 切开:纵向切开颈总至分叉上方
⑥ 剥离:剥离子/剪刀剥离斑块
⑦ 冲洗:肝素盐水冲洗远端反流
⑧ 缝合:补片缝合(推荐ePTFE/静脉补片)
⑨ 开放:开放顺序:ICA→ECA→CCA
补片缝合的重要性:可降低术后再狭窄率(补片组 vs 直接缝合:~5% vs ~15%)。
2. CAS 介入原则
CAS标准化步骤:
① 股动脉穿刺(Seldinger技术)
② 8F导引导管置入颈总动脉
③ 路径图下微导丝/微导管过斑块
④ 预扩张(直径偏小球囊,可选)
⑤ 定位:支架覆盖斑块全长
⑥ 释放:缓慢加压至命名压
⑦ 后扩张(如需要)
⑧ 颈内动脉保护装置(EPD):回收
⑨ 造影确认:残余狭窄<30%
栓塞保护装置(EPD)类型:
| 保护装置 | 特点 | 适应 |
|---|---|---|
| 远端滤网(Filter) | 捕获栓子,允许前向血流 | 大多数CAS |
| 远端阻塞球囊 | 完全阻塞,撤除栓子 | 颈内动脉迂曲 |
| 近端阻塞(Mo.Ma) | 颈总+颈外球囊 | 颈内动脉极重度狭窄 |
3. 机械取栓关键技术
ADAPT技术(首选):
① 6F长鞘/导引导管到位
② 中间导管(MAX)至病变近端
③ 微导管+微导丝通过闭塞段
④ 撤除微导管,留下微导丝
⑤ 抽吸导管沿导丝推送至血栓接触
⑥ 持续抽吸(60ml注射器/抽吸泵)
⑦ 推送抽吸导管同时维持负压
⑧ 撤管至体外,冲洗
SWIM技术(复杂病变):
① 支架(Solitaire 4×20mm)释放
② 中间导管跟进至支架近端
③ 负压抽吸同时撤出支架
④ 减少"踢腿"效应,提高首过效应
4. 脑出血外科治疗原则
开颅血肿清除(显微镜下):
| 原则 | 说明 |
|---|---|
| 早期手术 | 发病6-8小时内清除血肿 |
| 最小创伤 | 锁孔入路(keyhole)优先 |
| 功能保护 | 皮层造瘘<2cm,避开功能区 |
| 彻底止血 | 活动性出血点双极电凝 |
| 去骨瓣 | 大血肿、脑肿胀者同期去骨瓣 |
内镜下血肿清除(新兴技术):
优势:微创、视野好、手术时间短
步骤:
① 术前CT定位,额部马蹄形切口
② 颅骨钻孔→透明套筒置入
③ 内镜(0°/30°)直视下清除
④ 生理盐水冲洗,自动虹吸
⑤ 术后引流管(可不用)
5. 动脉瘤介入治疗原则
弹簧圈栓塞操作:
① 全麻、肝素化(ACT>250s)
② 3D-DSA测量:瘤体/瘤颈/工作角度
③ 微导管塑形(EZ 45°/S 3D)
④ 超选进入动脉瘤(最后显影)
⑤ 弹簧圈填塞(首圈成篮最重要)
⑥ 最后aim for Raymond分级 Ⅰ/Ⅱ
⑦ 即刻造影确认:Raymond Ⅰ(完全栓塞)
血流导向装置(FD)放置:
Pipeline Flex / Surpass Evolve 操作要点:
① 测量:载瘤动脉直径→选择FD尺寸
② oversizing:8-10%(太长优于太短)
③ 输送:微导管+输送导丝
④ 定位:覆盖瘤颈各1-2cm
⑤ 释放:缓慢牵拉外鞘
⑥ 按摩:球囊轻柔贴附(可选)
⑦ 抗血小板:双抗(阿司匹林+氯吡格雷)× 3-6月
介入术后抗血小板方案:
| 药物 | 方案 | 监测 |
|---|---|---|
| 阿司匹林 | 81-100mg QD 长期 | P2Y12 VerifyNow |
| 氯吡格雷 | 75mg QD × 3-6月 | P2Y12 PRU |
| 替格瑞洛 | 替代氯吡格雷(高反应者) | — |
六、第十期总结:六字口诀
| 要点 | 口诀/记忆 |
|---|---|
| CEA vs CAS选择 | 高风险解剖→CAS,低风险症状→CEA |
| 颈动脉阻断顺序 | E→C→I(外→总→内) |
| 取栓首选技术 | ADAPT(抽吸)→SWIM(补救) |
| 血肿手术指征 | 幕上>30ml,丘脑>15ml,小脑>15ml |
| 动脉瘤治疗时机 | 破裂→早期(<72h),未破裂→评估PHASES |
| 介入术后管理 | 双抗3-6月,定期影像随访 |
| ASPECTS评分 | M1-6+Cingu+Insula+Lent+ICA = 10分 |
七、下期预告
第十一期:脑血管病的一级预防与健康教育
- 高血压/糖尿病/高脂血症的管理目标
- 阿司匹林一级预防的争议与最新指南
- 颈动脉斑块的药物 vs 手术决策
- 生活方式干预(戒烟、运动、饮食)
上白泽慧音 · 2026-04-04